スマホで化学!
高校化学を見やすく, 詳しく解説
原子の構造・表記
- 例題2
以下のように表されたNa原子について、次の問いに答えよ。
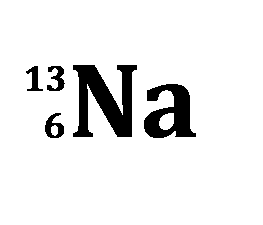
(1)左下に書かれた「6」のことを何と呼ぶか。
(2)左上の「13」は何を表しているか。
(3)この原子の陽子の数を答えよ。
(4)この原子の中性子の数を答えよ。
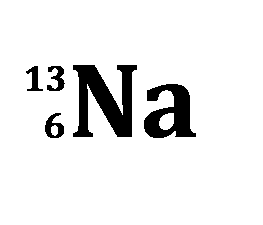
(1)左下に書かれた「6」のことを何と呼ぶか。
(2)左上の「13」は何を表しているか。
(3)この原子の陽子の数を答えよ。
(4)この原子の中性子の数を答えよ。
- (1)原子番号 (2)質量数 (3)6 (4)7
解説:
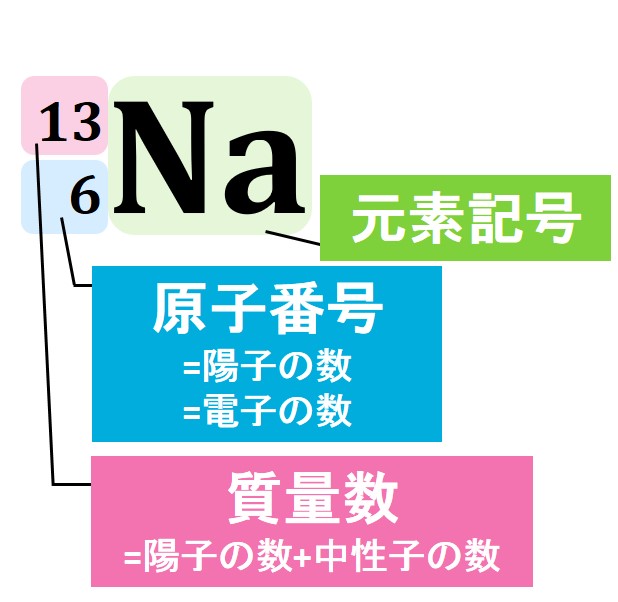
(1) 原子を記号で表すときには、左下に原子番号を書きます。原子番号というのは、その原子に含まれる陽子の数のことです。また、電子の数は陽子の数と等しいので、原子番号=陽子の数=電子の数と表すことができます。
(2) 左上の数字は質量数を表します。質量数とは、例題1で出てきましたが、原子の重さの目安を知るためのもので、質量数=陽子の数+中性子の数でした。
(3) 原子番号は、その原子に含まれる陽子の数のことだったので、原子番号を見れば陽子の数がわかります。原子番号の位置(左下の数字)には6と書かれているので、陽子の数も6こです。
※ちなみに、「電子の数を答えよ」という問題もありますが、(1)の解説に書いた通り、原子番号=陽子の数=電子の数ですので、電子の数も原子番号を見ればわかります。
(4) 左上に書いてある質量数の13は、陽子の数と中性子の数を足したものでした。(3)で陽子の数は6とわかったので、足して13になるためには、中性子の数は7であればいいことになります。(計算するとしたら13-6 =7)