スマホで化学!
高校化学を見やすく, 詳しく解説
最外殻電子と価電子
- 練習1
原子番号が17番の塩素Clについて、次の問いに答えよ。
(1) 最外殻電子の数はいくつか。
(2) Clの価電子数はいくつか。
(1) 最外殻電子の数はいくつか。
(2) Clの価電子数はいくつか。
- (1) 7個 (2) 7個
解説:
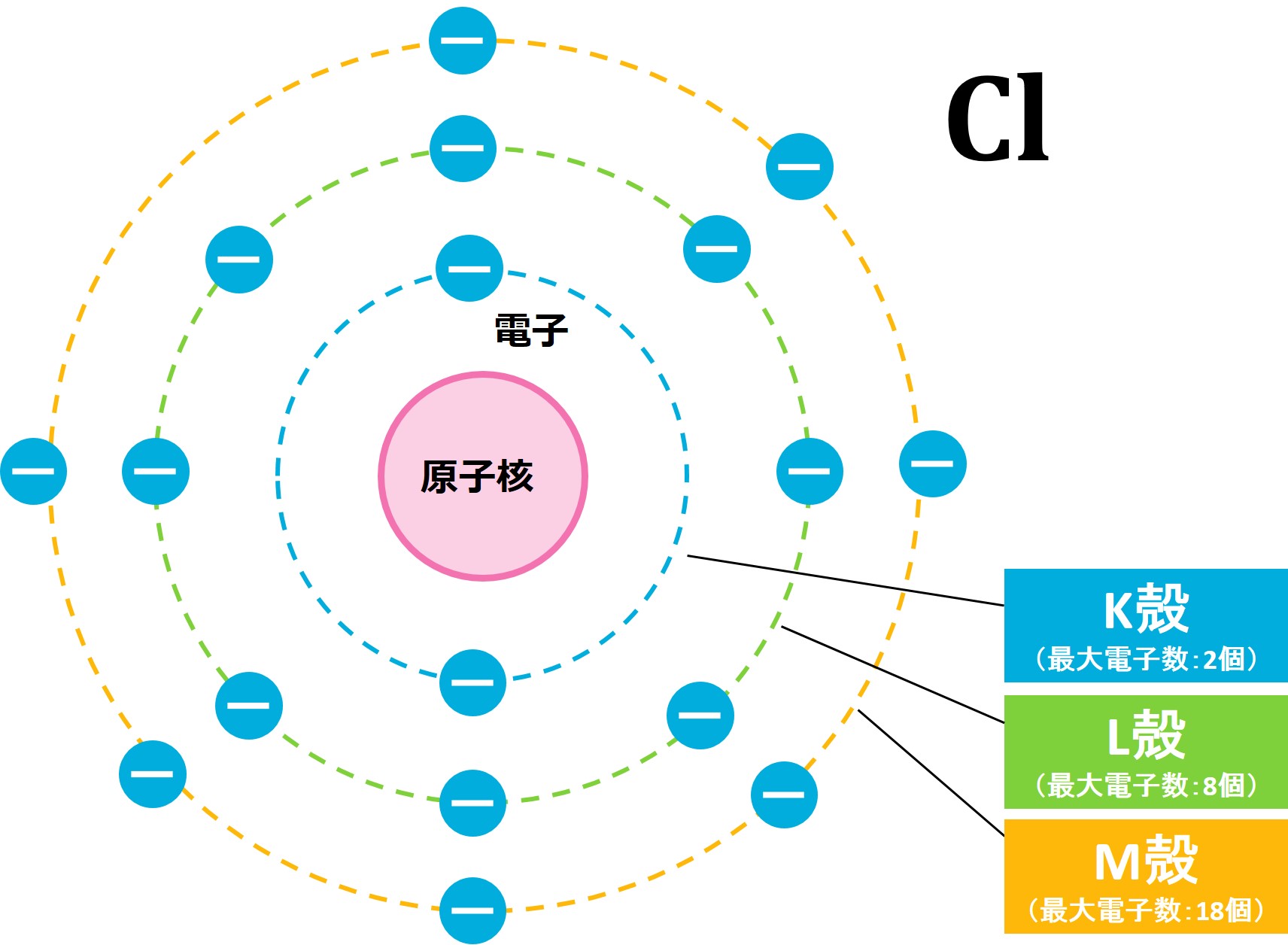
(1) 最外殻電子の数は、電子配置を書くことで求められます。そのために、まず、Clの電子の数を求めましょう。原子番号が17なので、電子の数は17個です(電子の数=原子番号)。次に電子配置です。内側の電子殻から順に17個の原子を配置していきます。
1番内側のK殻は最大電子数が2個なので、Cl原子が持つ17個の電子のうち、2個がK殻に配置されます。残りの電子は15個です。
2番目のL殻の最大電子数は8個なので、L殻に最大まで入れても7個あまります。このあまりをすべてM殻に入れれば電子配置の完成です。
電子配置を見ると、1番外側のM殻には電子が7個あるので、最外殻電子(1番外側にある電子の数)は7個です。
(2) 最外殻電子数が7個の時には、価電子数を0にする必要がないので、価電子数も最外殻電子数と同じ7個となります。
Point!
価電子数と最外殻電子数は基本的に同じ数!ただし、、、
◆最外殻に空きがないとき
◆最外殻電子数が8個のとき
には、価電子数を0とする