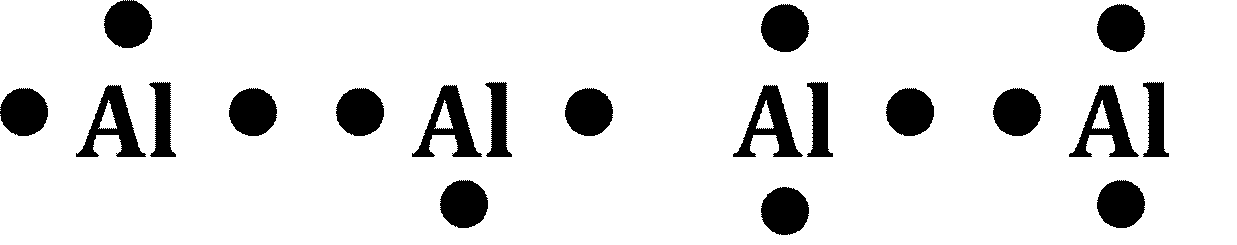スマホで化学!
高校化学を見やすく, 詳しく解説
電子式
- 例題1
原子番号が13番のAl原子を電子式で表せ。
電子式の書き方
電子式とは、最外殻電子を「●」で表したものです。(最外殻電子がわからない人はこちら)
下の図のように、「●」を書けるエリアは決まっていて、ここに最外殻電子の数だけ「●」を書き入れていきます。
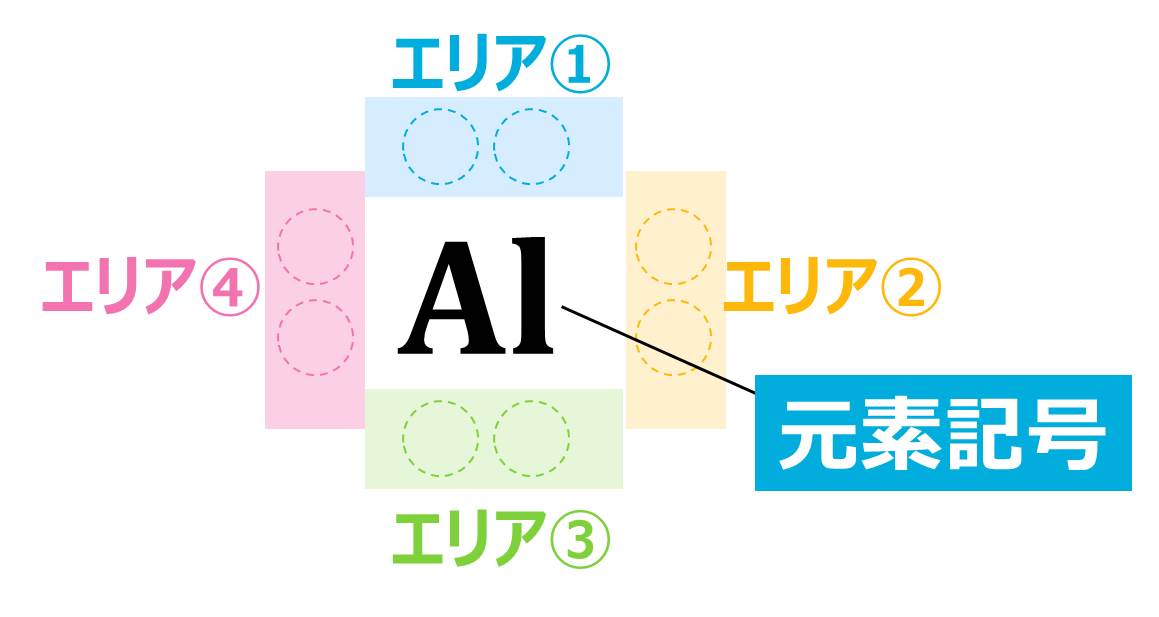
少し難しそうに見えますが、次の3つのルールだけ覚えておけば簡単に書けます。
Point!
電子式を書くときのルール①4つ目までは各エリアに1つずつ「●」を書いていく
※「●」を書く順番や位置に決まりはありません
②1つのエリアに書ける「●」は2つまで
③He(最外殻電子2つ)だけは、2つの「●」を同じエリアに書く(書くのはどのエリアでもOK)
解説:
例題のAlの電子式を考えましょう。電子式とは、最外殻電子を「●」で表したものでしたので、まずは電子配置を考えて、最外殻電子数を求めなければなりません。
原子番号が13なので、電子の数は13個です(電子の数=原子番号)。この13個の電子を内側の電子殻から順に配置していきます。
K殻は最大電子数が2個なので、Al原子が持つ13個の電子のうち、2個がK殻に配置されます。残りの電子は11個ですが、L殻の最大電子数は8個なので、L殻に最大まで入れても3個あまります。このあまりをすべてM殻に入れれば電子配置完了です。
この場合、一番外側にあるのはM殻で、そこには電子が3個あるので、最外殻電子は3個です。なので、電子式を書く場合には、元素記号「Al」の周りに「●」を3つ書けばOKです。
Point!で説明したように「4つ目までは各エリアに1つずつ「●」を書いていく」というルールがあったので、下の図のように各エリアに1つずつ「●」を書けば電子式が完成します。
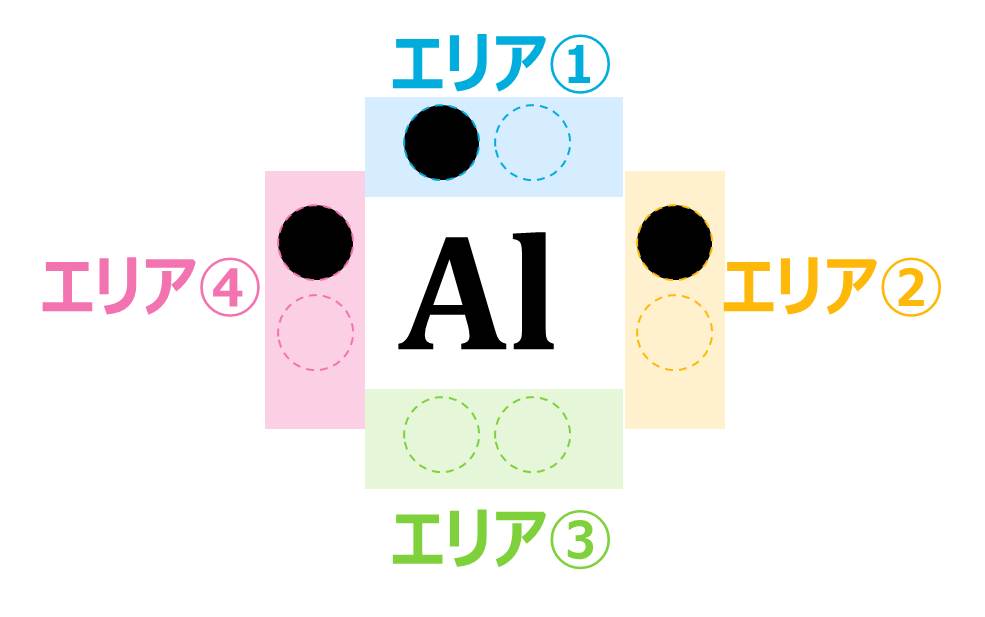
ただし、「4つ目までは各エリアに1つずつ書いていく」というルールさえ守っていれば、どのエリアから「●」を書き始めても良いので、Alの電子式は下のどれでも正解です。